对于携带BRCA1基因突变的女性而言,命运似乎总在“切除器官以绝后患”与“保留生育功能但承担巨大患癌风险”之间划下一道残酷的选择题。2025年底,好莱坞女星安吉丽娜·朱莉公开展示为防癌而切除乳腺留下的疤痕,再次将这一群体的困境置于公众视野。然而,一道来自生物医学工程领域的研究曙光,或许将彻底改写这道选择题的答案。2026年1月28日,国际顶级学术期刊《Cell》报道了北京航空航天大学作为第一完成单位在该领域取得的重大突破:一项名为POCKET的柔性可植入生物电子器件,有望让“朱莉”们不再面临“二选一”的绝境。
这项研究的起点,源自一个令妇产科医生深感无力的临床难题。对于遗传性卵巢基因突变(如BRCA1)的患者,临床指南通常建议预防性切除双侧卵巢和输卵管以杜绝癌症发生,但这意味着患者将永久丧失生育能力。传统的基因治疗技术,如病毒载体,在卵巢这类极度敏感的器官上被视为应用禁区,因为一旦操作不当,可能整合入生殖细胞基因组,甚至干扰人类基因库的稳定性。即便是常规的口服或静脉给药,也面临药物利用效率极低、毒副作用显著的困境。
卵巢表面崎岖不平,沟壑纵横,传统电穿孔器件无法实现 “高共形贴合”于器官表面,导致药物递送可控性差、效率低,无法从根本上精准治疗,解决这类“禁区难题”。
北京航空航天大学医学科学与工程学院常凌乾教授团队,联合机械工程及自动化学院徐晔教授团队另辟蹊径,从古老的“剪纸”艺术中获得了突破性灵感。他们创造性地提出了“器官定制化剪纸共形理论”,首次建立了剪纸结构几何参数与器官曲率、材料属性之间的定量关系。通过为器官进行三维扫描并智能生成最合身的“外衣”尺寸,团队利用飞秒激光技术将器件切割成彼此连接又相对独立的“碎片”,使其能通过微介入技术送达目标器官位置并进行组装。
最终,这款名为POCKET的器件在人体卵巢、眼球、肾脏等不同器官表面的有效覆盖率可超过95%,如同为器官穿上了一件量身定制的“电子外衣”,攻克了“高共形”与“高覆盖”不可兼得的难题。
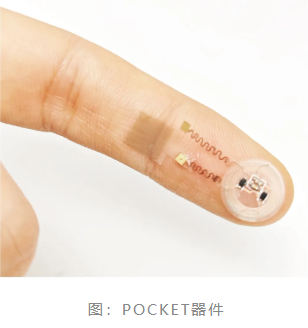
疗效验证
这件神奇的“电子外衣”并不仅仅是一件贴合的外衣。它采用四层功能化设计,通过纳米孔阵列薄膜与目标细胞形成精准的空间并列。在施加低电场时,高阻抗的纳米孔道产生显著的“纳米电穿孔”效应,在细胞膜上可逆、安全地打开小孔,同时驱动强大的电泳力,将药物或基因载荷的递送速度提升近千倍,从而实现高效率、高安全性的细胞内递送。
这一技术的疗效在多种动物模型中得到了有力验证。在模拟人BRCA1突变的小鼠模型中,POCKET成功将功能性BRCA1-Plasmid递送至全卵巢表面细胞(OSE)内。这不仅使小鼠的癌症发生率在一个治疗周期内降至零,还能刺激细胞分泌携带相关mRNA的外泌体,有效改善卵巢早衰症状。更重要的是,卵巢的激素分泌功能、卵子质量及生育能力均得到恢复,产生的后代健康。这一成果为携带致癌基因突变的女性提供了无需切除卵巢即可防癌、并保留生育力的全新选择。
内容来源:北京航空航天大学、中国科学报
责编:今路广
