2025年,妇科肿瘤抗体偶联药物(ADC)领域迈入靶点深耕与临床转化关键期,维替索妥尤单抗获批宫颈癌适应症,HER2、FRα等经典靶点研究再添重磅数据,新型靶点探索多点突破,国内专属专家共识同步落地,标志着该领域从临床探索走向规范化应用。妇产科网特邀苏州大学附属第一医院周金华教授,从ADC发展历程、靶点探索、未来革新三大维度,系统梳理年度核心进展,前瞻领域发展方向,为临床诊疗提供专业参考。
以宫颈癌(CC)、子宫内膜癌(EC)和卵巢癌(OC)为主的妇科肿瘤是威胁女性健康的一大类疾病。2022年我国女性宫颈癌发病率为21.81/10万,死亡率为8.06/10万;子宫体肿瘤发病率为11.25/10万,死亡率为1.96/10万;卵巢癌发病率为8.84/10万,死亡率为4.73/10万[1]。目前,妇科恶性肿瘤的治疗仍以手术、放疗和化疗为主。传统化疗缺乏肿瘤特异性、对正常细胞损伤大,严重的不良反应常使患者难以耐受,进而影响治疗效果[1,2]。
精准有效的靶向治疗是近年来临床研究和治疗更新的热点之一,但传统靶向治疗往往缺乏较强的细胞毒性,且易发生耐药。因此,如何精准地向目标肿瘤细胞输送细胞毒性药物,避免损伤正常细胞,是肿瘤药物治疗中待解决的难题。[2,3]
“魔法子弹”ADC类药物在妇科肿瘤中的探索
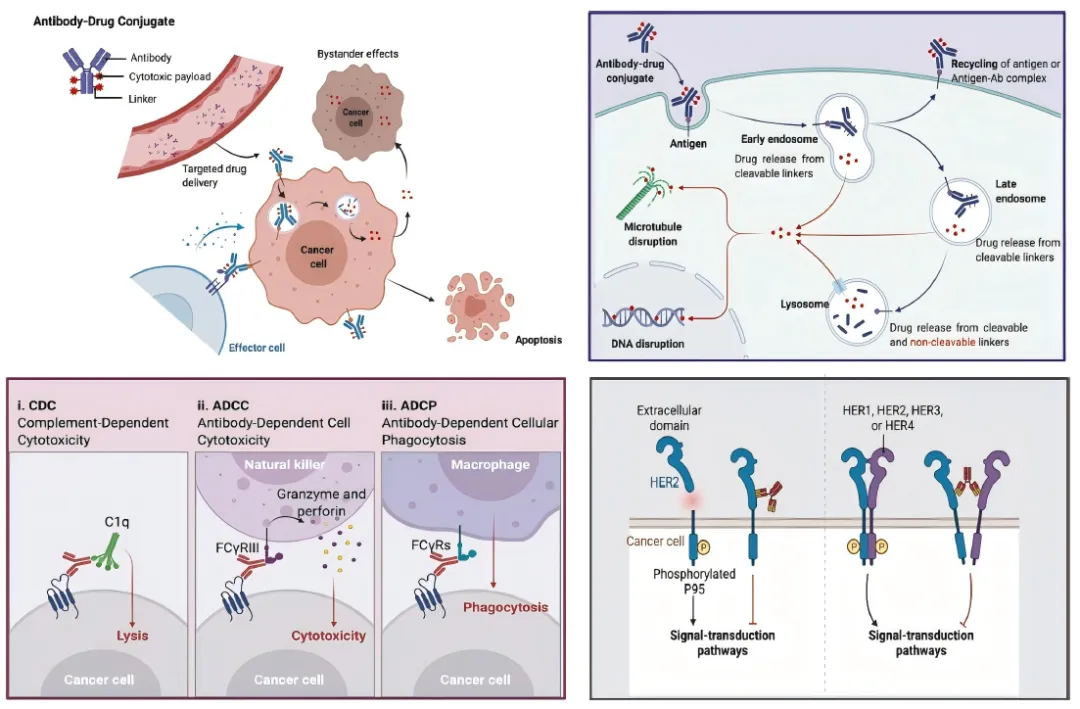
图1:ADC通过不同途径杀伤癌细胞的机制概述(左上)[25]。右上:ADC的主要核心作用机制;左下:ADC的抗体成分与免疫效应细胞结合,引发抗肿瘤免疫,包括补体依赖的细胞毒作用(CDC)、抗体依赖的细胞介导的细胞毒作用(ADCC)和抗体依赖的细胞吞噬作用(ADCP)效应;右下:ADC的抗体成分保留了其活性特征,因此可以干扰靶功能,抑制下游信号以抑制肿瘤生长
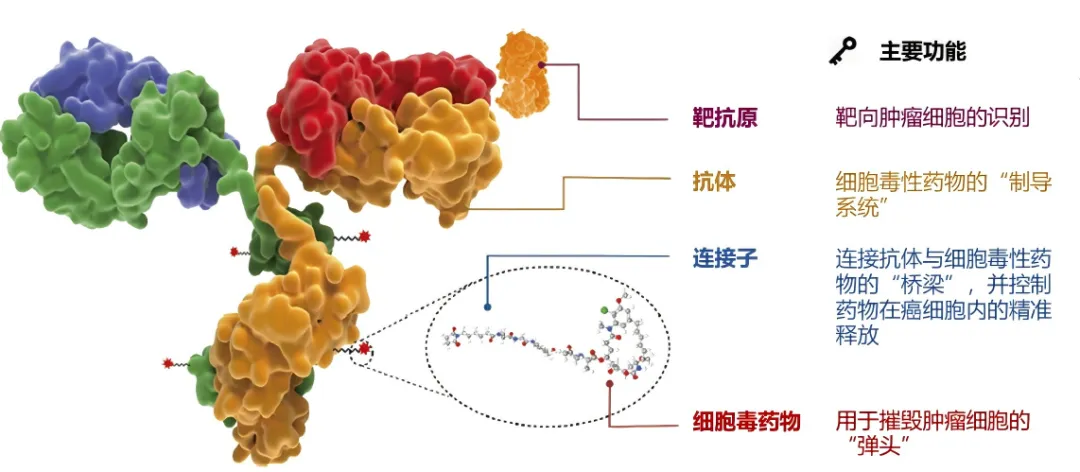
图2:ADC类药物的核心组成部分与特性[25]:靶抗原、抗体、连接子、细胞毒药物
抗体偶联药物(ADC)是一种新兴的治疗药物,随着对ADC类药物机制的不断深入了解和技术的更新与突破,目前全球已有16种ADC上市,其中7种在中国获批。妇科肿瘤ADC类药物的研发并不是孤立起步的,而是遵循了肿瘤分子特征驱动的拓展逻辑。早期ADC的成功主要集中在血液肿瘤、乳腺癌、胃癌、肺癌等大癌种,或许是出于肿瘤患者基数庞大,且通过免疫组化或基因检测可发现较高比例的靶点表达。药物疗效和安全性验证成功后,再根据分子特征的共性拓展至妇科肿瘤,是从“大癌种—分子特征—妇科肿瘤”的自然发展路径。ADC在妇科肿瘤领域也正在蓬勃发展,其中两种药物已获批上市(维替索妥尤单抗:2025年3月获批用于宫颈癌;索米妥昔单抗:2024年11月获批用于卵巢癌)。同时,多个临床试验正在进行,初步结果显示ADC在妇科肿瘤治疗中有较好的应用前景[2,3]。
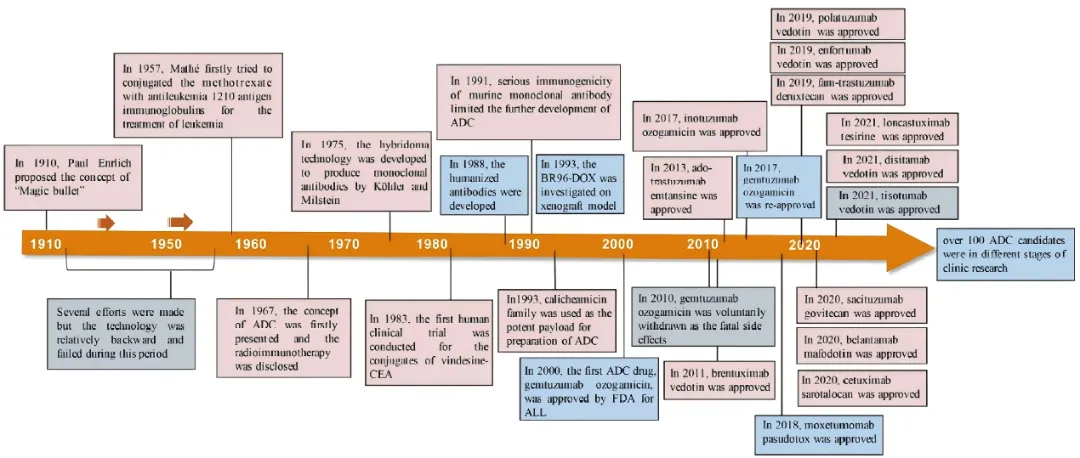
图3:“魔法子弹”ADC类药物开发和获批上市的时间线[25]。在我国,在妇科肿瘤领域获批适应症的ADC类药物有:索米妥昔单抗:2024年11月获批用于治疗既往接受过1-3线系统性治疗的叶酸受体α(FRα)阳性的铂类耐药卵巢癌(PROC);维替索妥尤单抗:2025年3月获批用于治疗系统性治疗期间或之后病情进展的复发或转移性宫颈癌患者
理想的ADC抗体应靶向仅在肿瘤组织中高表达,而在健康组织中低表达的肿瘤抗原。如人表皮生长因子受体2(HER2)在肿瘤中的表达较正常细胞高100倍。目前的靶点选择通常包括肿瘤细胞过表达的抗原或驱动基因编码的抗原,如叶酸受体α(FRα)、跨膜糖蛋白-2(Trop-2)、前列腺特异性膜抗原(PSMA)、间皮素(Mesothelin)、神经细胞黏附分子‑1(CD56)、CD70、脊髓灰质炎病毒受体相关蛋白4(Nectin4)、人表皮生长因子受体2(HER2)、表皮生长因子受体(EG⁃FR)等。[3]目前在妇科肿瘤中,ADC的研发集中于HER2、FRα、组织因子(TF)、Trop-2、B7-H4蛋白(B7 Homolog 4, VTCN1)、钠依赖性磷酸盐转运蛋白IIb(NaPi2b)、蛋白酪氨酸激酶7(PTK7)等[2,3]。相较化疗与免疫治疗,ADC具备更精准的杀伤与潜在更好耐受性,但不良事件谱较陌生且管理具有挑战;在妇科肿瘤(宫颈癌、子宫内膜癌、卵巢癌)中,ADC已在多项试验中提高客观缓解率(ORR)与无进展生存时间(PFS),但能否改变最终生存结局(OS)仍待验证与长期随访[4]。
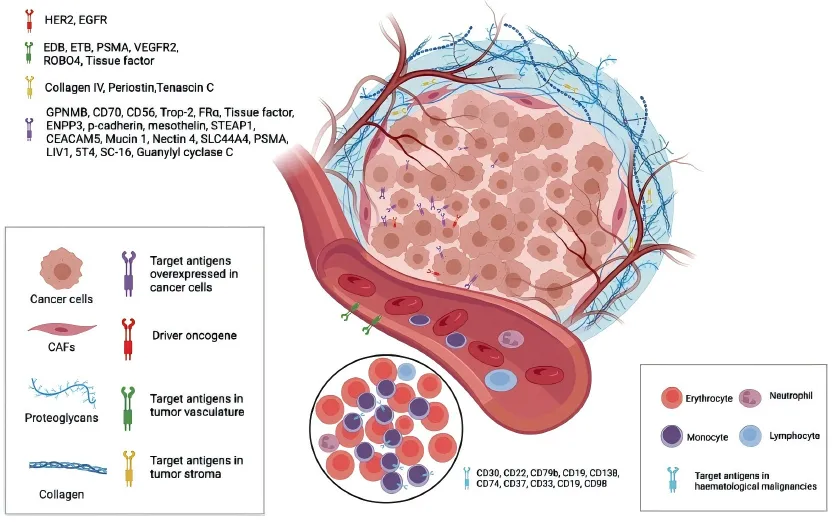
图4:基于肿瘤细胞(过表达及驱动基因相关)与肿瘤微环境(血管系统及基质)的重要靶抗原被用于抗体偶联药物的开发[25]
人表皮生长因子受体2(HER2)ADC
HER2作为经典的致癌驱动因子,是乳腺癌中最早、最典型的分子靶点之一,后发现胃癌中也存在较高比例的HER2扩增,DESTINY-Breast、DESTINY-Gastric系列研究加速了HER2靶向药物T-DXd在相关癌症治疗中的获批,而肺癌中HER2突变和扩增也将HER2药物的研究扩展至肺癌方向(DESTINY-Lung)。随着分子病理学研究的深入,人们发现约近一半子宫内膜浆液性癌存在HER2高表达或扩增,这种异常常提示不良预后。基于乳腺癌和肺癌HER2 ADC的成功经验,相关药物扩展至妇科肿瘤。德曲妥珠单抗(T-Dxd,DS8201a)、维迪西妥单抗(RC48)、瑞康曲妥珠单抗(SHR-A1811)等HER2 ADC已在妇科肿瘤人群相关临床试验中显示出初步疗效,HER2靶向也因此实现了从大癌种到妇科肿瘤的跨癌种发展[2]。
DESTINY-PanTumor02(NCT04482309)是一项全球、多中心、多队列、开放标签、在实体瘤患者中进行的Ⅱ期试验,纳入了HER2过表达(IHC 3+或2+)妇科肿瘤患者(子宫内膜癌队列n=40,宫颈癌队列n=40[包含5例IHC 1+患者],卵巢癌队列n=40),无论是哪种妇科肿瘤患者,德曲妥珠单抗(T-Dxd,DS8201a)治疗IHC 3+患者ORR均优于IHC 2+患者。子宫内膜癌患者全人群ORR达到57.5%,宫颈癌患者达到50%,卵巢癌患者达到45%,在ORR方面远超纳入的其他实体瘤患者[5]。在2025欧洲肿瘤内科学会年会(ESMO)上DESTINY-PanTumor02也公布了患者PFS和OS数据:子宫内膜癌患者全人群中位PFS达到11.1个月,宫颈癌患者7.0个月,卵巢癌患者5.9个月;宫内膜癌患者全人群中位OS达到24.3个月,宫颈癌患者13.6个月,卵巢癌患者13.2个月[6]。正是基于DESTINY-PanTumor02等研究的强有力数据,美国食品药品监督管理局(FDA)于2024年4月加速批准了德曲妥珠单抗用于治疗既往接受过系统性治疗且无满意替代方案的不可切除或转移性HER2阳性实体瘤患者。另一项STATICE(NCCH1615)[7]研究发现德曲妥珠单抗治疗HER2高表达与HER2低表达的子宫肉瘤(包括子宫平滑肌肉瘤样/癌肉瘤)中均显示较高ORR(HER2高表达约54.5%,HER2低表达约70%),提示旁观者效应可能使HER2低表达患者也获益。因为德曲妥珠单抗在妇科肿瘤的优越表现,继DESTINY-PanTumor02,还开展了专门针对中国人群的DESTINY-PanTumor03研究(Ⅱ期开放、多中心研究,纳入妇科肿瘤IHC 3+/2+/1+患者,NCT06271837)以及在子宫内膜癌患者中开展的DESTINY-Endometrial01研究(全球多中心、开放标签、随机对照Ⅲ期临床试验,NCT06989112)。
RC48-C018研究(RC48-C018)是一项纳入了HER2表达妇科恶性肿瘤的开放标签、多中心、Ⅱ期篮子研究。2024美国临床肿瘤学会年会(ASCO)上公布了维迪西妥单抗治疗复发或转移性宫颈癌患者(队列1,n=30)的结果[8]:26例有疗效的患者中,经确认的客观缓解率(cORR)为26.9%,确认的疾病控制率(cDCR)为80.8%;21例患者的中位PFS为4.37个月,中位OS为12.68个月,12个月OS率为57%。2025 ASCO大会发表了另一项名为Diversity的单臂、开放标签、多中心Ⅱ期研究,旨在探索维迪西妥单抗联合卡铂±贝伐珠单抗在HER2表达铂敏感卵巢癌患者中的疗效(n=10,NCT06420973)[9]:在10例患者中评估疗效,中位随访时间为3.2个月,ORR:70%,DCR 100%。
德曲妥珠单抗治疗IHC3+或2+妇科肿瘤患者、维迪西妥单抗治疗HER2表达复发或转移性宫颈癌患者均已被《妇科肿瘤抗体偶联药物临床应用专家共识》[10]收录并推荐。
除上述两种HER2 ADC外,2025 ASCO大会上还公布了另一项新型靶向HER2 ADC瑞康曲妥珠单抗在HER2表达晚期妇科肿瘤中的Ⅱ期研究结果[11],该研究是一项剂量探索研究,患者接受瑞康曲妥珠单抗4.8或6.4mg/kg(Q3W,Ⅳ),主要终点是RECISTv1.1标准规定的ORR,共纳入108例患者(46例OC患者、27例EC患者和35例CC患者)。OC、EC和CC所有患者cORR分别为56.1%、50.0%和63.6%;中位PFS分别为8.5个月、5.6个月和10.7个月。在4.8mg/kg队列中,OC、EC和CC患者的cORR分别为56.8%、52.0%和61.3%,PFS分别为8.5个月、7.2个月和10.7个月。
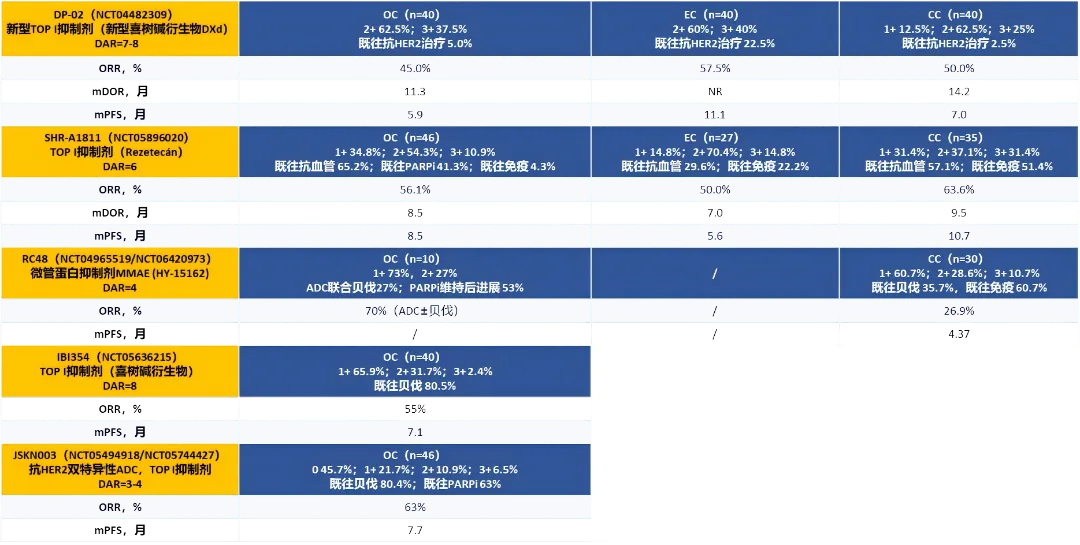
表1:已公布研究结果的靶向HER2 ADC类药物研究汇总
靶向HER2 ADC虽然给晚期妇科肿瘤患者带来了生存希望,但在治疗过程中需警惕间质性肺病。尽早与其他学科进行MDT以早期识别与管理间质性肺病并分级管理是行之有效的办法[12]。
叶酸受体α(FRα)ADC
叶酸受体α(FRα)在正常组织中几乎不表达,但在上皮性卵巢癌和部分子宫内膜癌中呈现高水平表达,且与肿瘤的恶性生物学行为相关。这种“肿瘤特异性”的分布格局为 ADC 提供了理想的安全窗口[2,3]。基于这一特征,由 FRα结合抗体与微管蛋白破坏药物美登木素DM4组成的索米妥昔单抗(MIRV)等FRα靶向ADC得以在卵巢癌人群中率先开展大规模临床试验,并最终实现了首个FRα ADC在既往接受过1-3线系统性治疗的FRα阳性铂耐药卵巢癌中的获批(Ⅱ期SORAYA研究[NCT04296890[13,14]],Ⅲ期MIRASOL研究[NCT04209855[15]])。
2025年FRα ADC的进展集中在以下两方面:1.新型FRα ADC药物(Luveltamab tazevibulin、Rinatabart Sesutecan和AZD5335);2.试图将获益患者从FRα≥75%拓展至≥25%,甚至无论FRα表达。
2025美国妇科肿瘤学会年会(SGO)上发布了一项名为REFRαME-O1试验(NCT05870748)的突破性口头报告[16],该研究探索了Luveltamab Tazevibulin(Luvelta)治疗FRα 表达≥25%铂类耐药卵巢癌患者的疗效。确定了luvelta的最佳剂量选择为5.2mg/kg+G-CSFx2个周期,然后4.3mg/kg治疗,ORR为32%。
2025 SGO、ASCO和ESMO大会上同样也发布了Rinatabart sesutecan(Rina-S®)的一项I/Ⅱ期剂量拓展队列B的结果(RAINFOL-01研究,NCT05579366[17]):无论FRα表达,在晚期卵巢癌中使用Rina-S 120mg/m²cORR为55.6%,Rina-S 100mg/m²cORR为22.7%[18];无论FRα表达,在晚期子宫内膜癌中使用Rina-S 100mg/m² cORR为50.0%,120mg/m² cORR为44.1%[19]。
FONTANA研究是一项针对晚期实体瘤患者开展的AZD5335首次人体研究(I/IIa期开放标签,NCT05797168),2025 ESMO大会上报告了AZD5335单药剂量优化(B1部分)的初步数据。B1部分入组既往治疗线数≤3线的铂耐药卵巢癌患者,根据FRα表达分组,分别接受AZD5335静脉注射,每3周一次,剂量优化设置为1.6、2.0和2.4mg/kg。截至2025年3月14日,中位治疗暴露时间为3.8个月,数据截止时仍在治疗的患者为107例(58.5%),高FRα表达(≥75%肿瘤细胞、染色强度≥2+,n=56):合并1.6、2.0、2.4mg/kg三个剂量水平的ORR为60.7%。低FRα表达(≥25%肿瘤细胞、染色强度≥1+,n=61):合并三个剂量水平的ORR为47.5%。[20]

表2:已公布研究结果的靶向FRα ADC类药物研究汇总
靶向FRα ADC在使用过程中需警惕眼毒性,索米妥昔单抗带来的眼毒性的发生多为脱靶效应导致的,在药物使用过程中建议患者预防性使用含糖皮质激素/润滑滴眼液、日常冷敷、血管收缩滴眼液及尽可能开展眼科MDT。[4,12]
其他靶向ADC类药物
TROP2是一种广泛存在于多种上皮性肿瘤细胞中的跨膜糖蛋白,在肿瘤增殖和侵袭过程中发挥作用,戈沙妥珠单抗(IMMU-132)在乳腺癌和尿路上皮癌中已获批。由于TROP2大多数子宫内膜癌中也存在较高表达[2],IMMU-132-01篮子研究(NCT01631552)开启了在妇科肿瘤领域的跨癌种探索[21]。研究共入组18例既往至少接受1次系统含铂化疗的转移性子宫内膜癌患者,戈沙妥珠单抗治疗ORR为22.2%,中位PFS为3.2个月,中位OS为11.9个月,观察到一定的缓解率和生存获益,不过数据仍然有限,尚需更多研究进一步验证其临床价值。
除上述主要靶点外,还有一些处于探索阶段的分子靶点正在获得更多的关注。CDH6在卵巢癌和肾癌中均有高表达,相关ADC处于早期试验;B7-H4作为免疫检查点分子,在卵巢癌和子宫内膜癌等妇科肿瘤中广泛高表达,且正常组织表达极低,因此成为近年来 ADC 开发的新兴方向[2,3],一项在首次在晚期实体瘤患者中的I/IIa期开放标签研究(BLUESTAR,NCT05123482)显示[22]:B7-H4 ADC Puxitatug samrotecan(AZD8205)在子宫内膜癌、卵巢癌和乳腺癌患者中获益持久,12周DCR率分别为75%、70.6%和58.3%。NaPi2b在超过90%的卵巢癌中阳性,而在正常组织中基本不表达,曾推动Lifastuzumab vedotin(LIFA)和 Upifitamab rilsodotin (UpRi)等 ADC 进入临床开发,尽管后续大规模试验结果未达预期或出现不可耐受的毒性使得研究被叫停[23],但仍显示了这一靶点的潜力[2,12]。这些探索性靶点的研究说明,妇科肿瘤 ADC 的开发正在不断拓展新方向,未来或将通过更精准的分子分型和患者筛选策略获得突破。
总结与展望
综上所述,妇科肿瘤ADC靶点的选择往往基于两方面:一是来自大癌种的先导经验,二是肿瘤组织本身的分子特征优势。除HER2、FRα、Trop‑2等表达阳性外,建议评估受体密度、内吞效率、旁观者效应、肿瘤微环境免疫特征,并结合现代AI技术,整合预测响应;但同时也需要关注药物可及性,推动伴随诊断标准化,从而选择优势患者,平衡药物疗效与患者综合疾病负担。[24]
在精准医疗成为癌症治疗主旋律的今天,ADC通过整合抗体的特异性和化疗药物的强效性,在妇科肿瘤的治疗中展示出巨大的潜力与广阔前景。未来的发展方向将包括优化靶点选择、改进连接子和载药结构以提高稳定性与释放精准度、联合免疫治疗或其他靶向药物延缓耐药发生,以及推广生物标志物检测以实现更加精准的患者筛选[10,23]。随着新一代ADC技术的不断完善和更多、更完善、更大样本量的临床试验证据的积累,ADC药物有望在妇科肿瘤治疗中为患者带来更高效、更安全的治疗方案。
参考文献:
[1] Han B, Zheng R, Zeng H, et al. Cancer incidence and mortality in China, 2022. J Natl Cancer Cent. 2024 Feb 2;4(1):47-53. doi: 10.1016/j.jncc.2024.01.006. PMID: 39036382; PMCID: PMC11256708.
[2] Xu D, Chen Z S, Peng X, et al. Research progress of antibody–drug conjugates in gynecologic cancer[J]. Holistic Integrative Oncology, 2024, 3(1): 42.
[3] 陆佩瑶, 陈丽华, 向阳. 抗体偶联药物在妇科肿瘤中的研究进展[J]. 肿瘤药学, 2025, 15(1): 10-20.
[4] Wang PH, Yang ST, Chang WH. Antibody-drug conjugates (ADCs) may be a big breakthrough in gynecologic cancer treatment (III): Understanding of ADC. Taiwan J Obstet Gynecol. 2025 Nov;64(6):935-937. doi: 10.1016/j.tjog.2025.09.003. PMID: 41213780.
[5] Meric-Bernstam F, Makker V, Oaknin A, et al. Efficacy and Safety of Trastuzumab Deruxtecan in Patients With HER2-Expressing Solid Tumors: Primary Results From the DESTINY-PanTumor02 Phase II Trial. J Clin Oncol. 2024 Jan 1;42(1):47-58. doi: 10.1200/JCO.23.02005. Epub 2023 Oct 23. PMID: 37870536; PMCID: PMC10730032
[6] Makker, V. et al. 957P Trastuzumab deruxtecan (T-DXd) for pretreated patients (pts) with HER2-expressing solid tumors: DESTINY-PanTumor02 (DP-02) part 1 final analysis. Annals of Oncology, Volume 36, S587 - S588
[7] Nishikawa T, Hasegawa K, Matsumoto K, et al. Trastuzumab Deruxtecan for Human Epidermal Growth Factor Receptor 2-Expressing Advanced or Recurrent Uterine Carcinosarcoma (NCCH1615): The STATICE Trial. J Clin Oncol. 2023 May 20;41(15):2789-2799. doi: 10.1200/JCO.22.02558. Epub 2023 Mar 28. PMID: 36977309; PMCID: PMC10414746.
[8] Guangwen Yuan, et al. Evaluation of the effectiveness and safety of disitamab vedotin in HER2-expressing 2L recurrent or metastatic cervical cancer (r/mCC): Interim results of RC48-C018.. J Clin Oncol 42, 5528-5528(2024).
[9] Tong Shu, et al. Preliminary analysis of disitamab vedotin combined therapy for HER2-expressing platinum-sensitive recurrent ovarian/peritoneal/fallopian tube cancer (Diversity study): A single-arm, multicenter phase II trial. 2025 ASCO Annual Meeting. Abstract #5564.
[10] 中国抗癌协会子宫体肿瘤专业委员会,中华医学会妇科肿瘤学分会.妇科肿瘤抗体偶联药物临床应用专家共识[J].现代妇产科进展,2025,34 (4):241-248. DOI:10.13283/j.cnki.xdfckjz.2025.04.001
[11] Beihua Kong et al. SHR-A1811 in patients (pts) with HER2-expressing advanced gynecological cancers (Gynecol C): A phase 2 study. 2025 ASCO Annual Meeting. Abstract #5612.
[12] Sato S, Shoji T, Jo A, et al. Antibody-Drug Conjugates: The New Treatment Approaches for Ovarian Cancer. Cancers (Basel). 2024 Jul 15;16(14):2545. doi: 10.3390/cancers16142545. PMID: 39061184; PMCID: PMC11275051.
[13] Matulonis UA, Lorusso D, Oaknin A, et al. Efficacy and Safety of Mirvetuximab Soravtansine in Patients With Platinum-Resistant Ovarian Cancer With High Folate Receptor Alpha Expression: Results From the SORAYA Study. J Clin Oncol. 2023 May 1;41(13):2436-2445. doi: 10.1200/JCO.22.01900. Epub 2023 Jan 30. PMID: 36716407; PMCID: PMC10150846.
[14] Coleman RL, Lorusso D, Oaknin A, et al. Mirvetuximab soravtansine in folate receptor alpha (FRα)-high platinum-resistant ovarian cancer: final overall survival and post hoc sequence of therapy subgroup results from the SORAYA trial. Int J Gynecol Cancer. 2024 Aug 5;34(8):1119-1125. doi: 10.1136/ijgc-2024-005401. PMID: 38858103; PMCID: PMC11347190.
[15] Moore KN, Angelergues A, Konecny GE, et al. Mirvetuximab Soravtansine in FRα-Positive, Platinum-Resistant Ovarian Cancer. N Engl J Med. 2023 Dec 7;389(23):2162-2174. doi: 10.1056/NEJMoa2309169. PMID: 38055253.
[16] Jung-Yun Lee, et al. Efficacy and safety of luveltamab tazevibulin in patients with recurrent platinum-resistant ovarian cancer: results from the dose-optimization stage of the REFRαME-O1 (GOG-3086, ENGOT-79OV, and APGOT-OV9) phase 2/3 study. 2025 SGO.
[17] Rinatabart sesutecan (Rina-S) for advanced solid tumors (GCT1184-01/ PRO1184-001) (PRO1184-001). ClinicalTrials.gov. Updated March 4, 2025. Accessed March 17, 2025. https://clinicaltrials.gov/study/NCT05579366
[18] Lee EK, Yeku O, Winer I, et al. Rinatabart sesutecan (Rina-S) for patients with advanced ovarian cancer: results from dose expansion cohort B1 of a phase 1/2 study. Presented at: 2025 SGO Annual Meeting on Women’s Cancer. March 14-17, 2025; Seattle, WA. Abstract 809034.
[19] Ira Winer, et al. Rinatabart sesutecan (Rina-S) for patients with advanced endometrial cancer: First disclosure from dose expansion cohort B2 of the GTC1184-01 study. 2025 ASCO Annual Meeting. Abstract #3039./ Cloven, N. et al. 1121P Rinatabart sesutecan (Rina-S®) for patients with advanced or recurrent endometrial cancer (a/r EC): Update from dose expansion cohort B2 of RAINFOL™-01. Annals of Oncology, Volume 36, S700
[20] Oaknin, A. et al. 1065MO First-in-human study of AZD5335, a folate receptor α (FRα)-targeted antibody-drug conjugate, in patients with platinum-resistant recurrent ovarian cancer. Annals of Oncology, Volume 36, S669 - S670
[21] Bardia A, Messersmith WA, Kio EA, et al. Sacituzumab govitecan, a Trop-2-directed antibody-drug conjugate, for patients with epithelial cancer: final safety and efficacy results from the phase I/II IMMU-132-01 basket trial. Ann Oncol. 2021 Jun;32(6):746-756. doi: 10.1016/j.annonc.2021.03.005. Epub 2021 Mar 16. PMID: 33741442.
[22] Meric-Bernstam, F. et al. 606O Initial results from a first-in-human study of the B7-H4-directed antibody-drug conjugate (ADC) AZD8205 (puxitatug samrotecan) in patients with advanced/metastatic solid tumors. Annals of Oncology, Volume 35, S485 - S486
[23] He J, Chen M, Jia L, et al. Antibody-drug conjugates in gynecologic cancer: current landscape, clinical data, and emerging targets. Int J Gynecol Cancer. 2025 Sep;35(9):101978. doi: 10.1016/j.ijgc.2025.101978. Epub 2025 Jun 19. PMID: 40743868.
[24] Koshkimbayeva G, Amirkhanova A, Orazymbetova A, et al. Recent therapeutic advances in gynecologic oncology: evolving roles of immunotherapy, antibody-drug conjugates, and clinical trial innovations. Front Oncol. 2026 Jan 15;15:1697180. doi: 10.3389/fonc.2025.1697180. PMID: 41626151; PMCID: PMC12851983.
[25] Fu Z, Li S, Han S, et al. Antibody drug conjugate: the "biological missile" for targeted cancer therapy. Signal Transduct Target Ther. 2022 Mar 22;7(1):93. doi: 10.1038/s41392-022-00947-7. PMID: 35318309; PMCID: PMC8941077.
专家简介

周金华 教授
苏州大学附属第一医院
主任医师,教授,博士生导师,博士后合作导师
苏州大学附属第一医院妇产科 科副主任,第一党支部书记
❖MD Anderson癌症中心博士后
❖江苏省临床重点专科 学科带头人
❖中华医学会妇科肿瘤分会 青年学组成员
❖中国医师协会妇产科分会宫颈病变学组成员
❖中国临床肿瘤学会(CSCO)妇科肿瘤专委会 委员
❖江苏省医学会妇产科分会 常务委员
❖江苏省研究型医院学会妇科肿瘤专委会 副主任委员
❖江苏省抗癌协会妇科肿瘤专业委员会 副主任委员
❖苏州市医学会妇产科分会 副主任委员
❖苏州市医学会妇科肿瘤分会 副主任委员
❖苏州市妇科医疗质控中心 副主任
❖江苏省“333人才工程”培养对象
❖“四大慢病”国家科技重大专项 项目骨干,先后主持国家自然科学基金项目4项,第一/通讯作者(含共同)发表SCI论文30篇,影响因子累计超200分,10分以上5篇
责编:霍盼
