对于晚期卵巢癌患者来说,“试错式治疗”是临床一大痛点。化疗耐药、PARP抑制剂无效,不仅延误治疗时机,还可能加重患者身心负担。重庆大学附属肿瘤医院妇科肿瘤中心邹冬玲教授团队最新发表在《Journal of Translational Medicine》的研究给出了破解方案:患者来源类器官(PDOs)能精准复刻肿瘤特性,提前预判化疗和PARP抑制剂的治疗反应,为卵巢癌个性化治疗提供“试药导航”!
类器官:复刻肿瘤的“迷你替身”
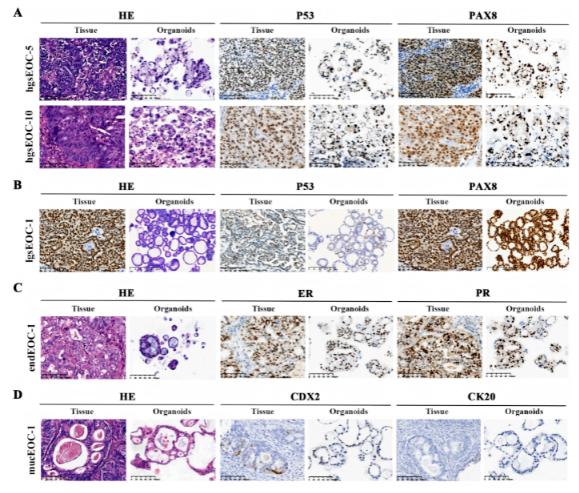
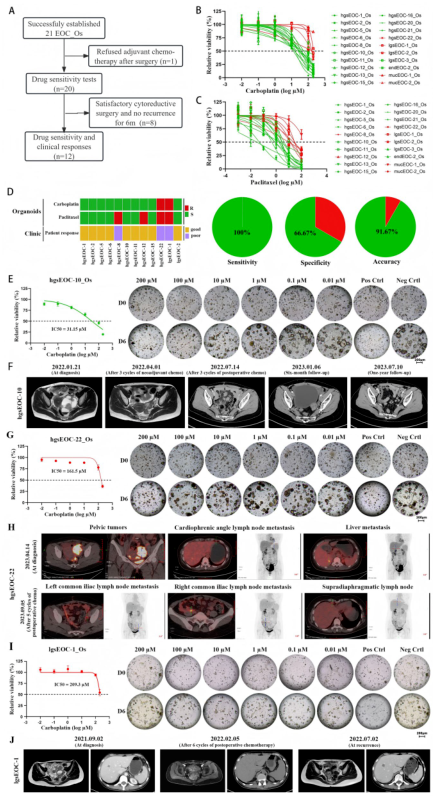
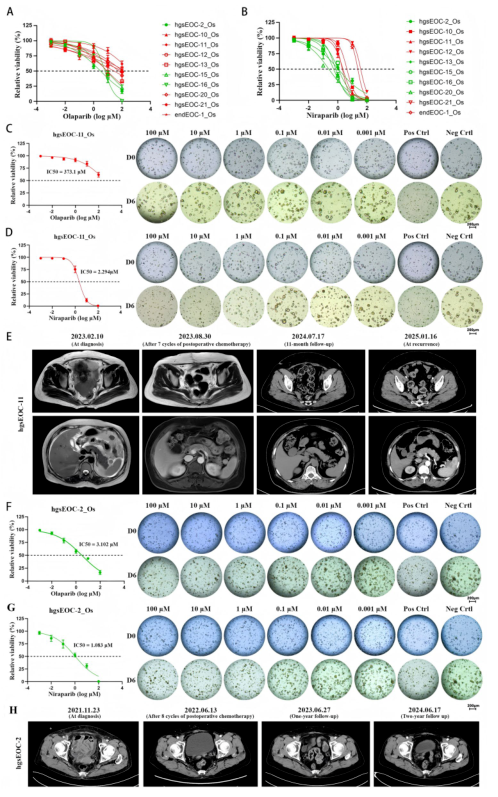
图1:研究流程+类器官形态示意图 卵巢癌之所以难治,核心在于其高度异质性,即使病理类型相同,不同患者的治疗反应也可能天差地别。传统的细胞系、动物模型难以还原这种个体差异,而患者来源类器官完美解决了这一难题。 研究团队从30名初治晚期卵巢癌患者的肿瘤组织中,成功构建了21个类器官模型,成功率达70%。这些“迷你肿瘤”不仅在显微镜下呈现出与原发肿瘤一致的形态特征。比如高浆液性癌的囊性结构、子宫内膜样癌的腺体排列,还精准保留了肿瘤的分子蓝图: ★90.9%的高浆液性癌类器官携带TP53突变,与临床常见突变特征一致; ★子宫内膜样癌类器官保留了PTEN突变等亚型标志性改变; ★肿瘤突变负荷(TMB)与原发肿瘤高度相关,相关系数高达0.9967。 图2:类器官与原发肿瘤的病理+免疫表型对比图 简单说,每个患者的类器官都是其肿瘤的“精准替身”,为个性化疗效预测提供了最贴近临床的模型基础。 化疗疗效预判:准确率91.7%,避免无效治疗 图3:化疗药敏检测+临床疗效对应图 卡铂+紫杉醇是卵巢癌一线化疗金标准,但仍有部分患者对其耐药。研究中,团队用类器官对这一化疗方案进行敏感性测试,并与患者临床结局对比,结果令人振奋: 类器官预测化疗反应的准确率达91.67%,其中敏感性100%、特异性66.67%,AUC值高达0.95。 具体来看: ★对化疗敏感的类器官,对应的患者在临床治疗中均获得显著疗效,肿瘤缩小、CA125水平大幅下降,术后随访6个月以上无复发; ★而类器官显示耐药的患者,临床中果然出现化疗无效,有的血清CA125持续升高,有的肿瘤未缩小甚至进展,最终被诊断为铂类难治性卵巢癌; ★低级别浆液性癌、黏液性癌的类器官普遍表现出化疗耐药,与这类亚型临床化疗效果不佳的特点完全吻合。 这意味着,通过类器官“试药”,医生可以提前筛选出对化疗敏感的患者,避免为耐药患者开具无效方案,让治疗从“盲目尝试”转向“精准匹配”。 PARP抑制剂疗效:突破基因检测局限 PARP抑制剂的出现,让卵巢癌治疗进入靶向时代,但传统的基因检测(如 BRCA突变、HRD评分)并非完美。部分HRD阳性患者对PARP抑制剂无效,而有些HRD阴性患者却能从中获益。 图4:上皮性卵巢癌类器官的PARP抑制剂敏感性检测及临床影像学验证 研究中,类器官成功破解了这一临床困惑: ★1例HRD阳性患者的类器官对奥拉帕利、尼拉帕利均耐药,临床中该患者接受PARP抑制剂维持治疗后,仅15个月就出现复发,符合“耐药”判断; ★2例HRD阴性、BRCA野生型患者的类器官显示对PARP抑制剂敏感,其中1例患者临床持续获益32个月,至今仍处于完全缓解状态; 这一发现证实,类器官能提供基因检测无法捕捉的“功能层面”信息,弥补了单纯基因组分析的局限性,让PARP抑制剂的适用人群筛选更精准。 临床价值:从实验室走向诊疗一线 这项来自重庆大学附属肿瘤医院的研究,不仅为卵巢癌疗效预测提供了新工具,更让精准治疗有了可落地的路径: ★初诊患者:手术或活检后构建类器官,1-2周内完成化疗+PARP抑制剂敏感性测试,为一线治疗方案制定提供直接依据; ★复发患者:需采集复发时的肿瘤组织构建类器官,精准复刻复发灶的异质性与耐药新特征,避免沿用初诊组织或方案导致的预判偏差,为挽救治疗快速筛选最优方案; ★罕见亚型:成功构建卵巢癌肉瘤、小细胞癌等罕见亚型的类器官,为这类缺乏标准治疗方案的患者提供个性化测试平台。 展望:未来治疗的“精准导航” 随着类器官技术的成熟,晚期卵巢癌的治疗模式正悄然改变,从“按指南用药”到“按个体模型用药”,从“经验性选择”到“数据化预判”。未来,随着多中心验证、技术标准化的推进,类器官有望成为卵巢癌诊疗的常规手段,让每一位患者都能避开无效治疗的弯路,精准匹配最优方案。 对于妇产科医生而言,这一技术让临床决策更有底气;对于卵巢癌患者来说,这意味着更多生存希望。卵巢癌的精准治疗时代,正由“迷你肿瘤”的精准预判拉开序幕! 内容来源:《JTM》 审核:邹冬玲教授团队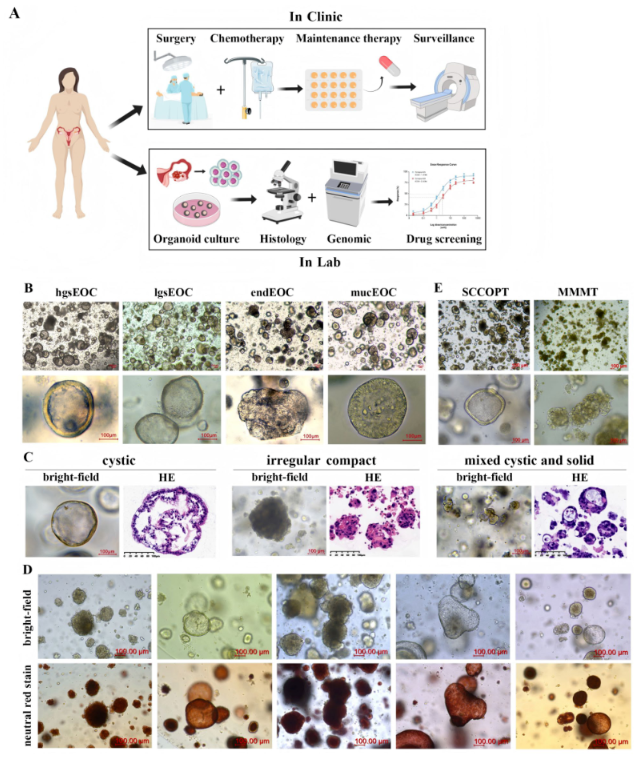
责编:今路广
